Часто пациенты с инфарктом миокарда умирают не от самого инфаркта, а от его осложнений.
Осложнения инфаркта миокарда включают в себя:
- ишемические осложнения: стенокардия, расширение зоны инфаркта;
- механические осложнения: сердечная недостаточность, кардиогенный шок, дисфункция митрального клапана, аневризмы, ;
- аритмии — предсердные, желудочковые и другие виды;
- тромбоз и эмболию;
- воспалительные осложнения — перикардит;
- психосоциальные осложнения (в том числе депрессии).
Смертность после инфаркта остается высокой, и чаще всего она наступает от аритмии. Разберемся подробнее с основными видами осложнений.
Ишемические осложнения
У пациентов с расширением зоны инфаркта или с постинфарктной стенокардией обычно возникает непрерывная или периодическая боль в груди, а иногда на электрокардиограмме появляются новые изменения. При подозрении на недуг пациентам делают эхокардиографию.
После инфаркта миокарда при постоянных ишемических симптомах проводят медикаментозную терапию с аспирином, гепарином, нитратами и бета-адреноблокаторами.
Повторный инфаркт, случившийся в течение первых 2 суток после первого, трудно диагностировать. Чаще он встречается у больных с сахарным диабетом.
Постинфарктная стенокардия может возникать в период от нескольких часов после инфаркта до месяца.
Механические повреждения
Осложнения инфаркта миокарда, вызванные механическими причинами, включают в себя ряд серьезных поражений:
- сердечная недостаточность;
- нарушения функций левого желудочка;
- кардиогенный шок (сложный симптом, связанный с поражением сердца, почек и головного мозга);
- разрыв стенки желудочка или перегородки между желудочками;
- аневризмы и ложные аневризмы;
- недостаточность правого желудочка;
- повреждения митрального клапана.
После инфаркта может возникнуть дисфункция левого желудочка или сердечная недостаточность. Выраженная сердечная недостаточность после разрыва сердца свидетельствует о неблагоприятном прогнозе.
Сердечная недостаточность возникает из-за повреждения самого миокарда во время инфаркта, но может быть вызвана аритмией или механическими осложнениями, например, дефектами митрального клапана или межжелудочковой перегородки. Тяжесть сердечной недостаточности зависит от степени инфаркта и наличия каких-либо других осложнений.
Другим механическим осложнением острой болезни является кардиогенный шок. Он возникает у 5-20% пациентов, пострадавших от разрыва сердца. Его тяжесть определяется различимыми хрипами в легочных полях и слышимостью тонов сердца.
Сердечная недостаточность, как правило, хорошо реагирует на кислород, диуретики и внутривенное введение нитратов. Пациенты с клиническими признаками сердечной недостаточности и диабетом должны получать Эплеренон или Спиронолактон, второе лекарство дешевле, но имеет больше побочных эффектов. Пациенты получают дополнительно кислород, а при очень тяжелой сердечной недостаточности может потребоваться операция. Если она невозможна, то вероятность смертельного исхода составляет более 70%.
Еще одно механическое осложнение — разрыв межжелудочковой перегородки или стенки желудочка. Это событие случается нечасто, но является опасным для жизни. Факторы риска этого осложнения: пожилой возраст, женский пол. Часто такое осложнение возникает при повышении частоты сердечных сокращений при поступлении или при повышенном кровяном давлении.
Данное осложнение может развиться уже через 24 часа после инфаркта миокарда, но часто случается через 2-7 дней после него. Уровень смертности превышает 90%.
Случается постинфарктный разрыв межжелудочковой перегородки.
Вначале у пациентов могут отсутствовать какие-либо значительные сердечно-легочные симптомы, но потом быстро развивается стенокардия, шок или отек легких и другие симптомы. Признаком разрыва желудочковой перегородки могут быть жесткие звуки у левого нижнего края грудины. На эхокардиограмме заметен рост насыщения кислородом правого желудочка. Постинфарктный дефект желудочковой перегородки требует срочного хирургического вмешательства.
При разрыве стенки возникает кровотечение в перикард, что приводит к закупорке сердца с прогрессированием недостатка сердечной функции. Нередки случаи смертельного исхода. При этом осложнении надежда только на хирургическую операцию.
Иногда возникают ложные аневризмы стенки левого желудочка. Они могут оставаться клинически незамеченными и обнаруживаться только при обычных исследованиях, но у некоторых пациентов следствием является сердечная недостаточность и аритмия. Диагноз подтверждается с помощью эхокардиографии, МРТ или КТ. Примерно в трети случаев может произойти спонтанный разрыв ложной аневризмы, поэтому хирургическое вмешательство рекомендуется всем пациентам.
Повреждение митрального клапана может быть связано с ишемией, некрозом или разрывами. Дефекты митрального клапана после инфаркта миокарда дают плохой прогноз, но часто носят временный характер и протекают бессимптомно. Необходимо сделать эхокардиографию, чтобы подтвердить диагноз, особенно в том случае, если требуется отличить его от разрыва межжелудочковой перегородки, а также для оценки тяжести повреждения. Иногда разрыв требует замены митрального клапана. Перед операцией проводят коронарографию.
У некоторых пациентов возникает постинфарктная аневризма левого желудочка. Частота таких событий составляет 2-15%. Пятилетняя выживаемость при этом отмечается в 10-25% случаев. Рентгенограмма может показывать ненормальную выпуклость на левой границе сердца, но окончательная диагностика проводится с помощью эхокардиографии, МРТ и КТ. При аневризме может возникнуть застойная сердечная недостаточность. Пациенты получают ингибиторы АПФ, дигоксин и диуретики. В случае настенных тромбов показана антикоагуляция с варфарином.
Тяжелая сердечная недостаточность и желудочковые аритмии у больных с аневризмами являются показаниями для хирургической операции.
Осложнения после инфаркта во многих случаях ведут к недостаточности правого желудочка. Это расстройство проявляется пониженным давлением, венозным вздутием при ясных легких и отсутствии одышки. Тяжелая форма может приводить к изменению психики. Диагностика проводится с помощью эхокардиографии. Следует избегать нитратов, диуретиков и аналогичных лекарств. Лечение сводится к поддержке заполнения желудочков жидкостью, назначаются инотропы, например, добутамин. У большинства больных после острого поражения состояние правого желудочка улучшается в течение 2-3 суток.
По разным причинам может произойти обструкция путей оттока из левого желудочка: из-за гипертрофии левого желудочка, кровотечения, обезвоживания, дефектов митрального клапана, стрессов, беспокойства, лекарств. Это редкое осложнение. Тест для диагностики — эхокардиография.
Аритмии
Опасная для жизни аритмия (например, или общая блокада) может быть первым проявлением ишемии. Аритмия приводит ко многим зарегистрированным случаям внезапной сердечной смерти. Нарушение ритма сердца, происходящее в первые 2 суток после инфаркта, не зависит от его степени. Поздние аритмии, возникающие на третьи сутки и позже, зависят от степени поражения желудочков. Риск смерти от аритмии является самым высоким в течение первых 6 месяцев после инфаркта миокарда и остается на высоком уровне в течение последующих 2 лет.
Аритмии могут быть вызваны самим инфарктом, токсическими продуктами, нарушением метаболизма (особенно дисбалансом калия или магния). Некоторые случаи аритмии (например, желудочковая тахикардия) не требуют лечения. Не следует лечить незначительные нарушения ритма. Но серьезные нарушения, особенно у пожилых пациентов, нельзя пропустить. Их симптомами являются боль, ацидоз, гипоксия.
Раннее лечение аритмий может предупредить кардиогенный шок, приводящий к необратимым повреждениям миокарда.
Блокада сердца и нарушения проводимости часто носят временный характер. может возникнуть из-за боли, тревоги или лекарств.
При желудочковой аритмии пациентам назначают адреналин, амиодарон или бета-блокаторы внутривенно, а также магний.
Тромбоз и эмболия
Осложнения инфаркта миокарда в форме тромбоза глубоких вен и эмболии легких в настоящее время случаются сравнительно редко, чаще у тех пациентов, которые находятся в постели из-за сердечной недостаточности. Смертность от этого осложнения составляет около 3% и случается в течение первой-третьей недели после инфаркта.
Для профилактики используют низкомолекулярный гепарин и компрессионные чулки.
Эхокардиография может выявить внутрижелудочковые тромбы. Тромбы возникают как осложнение инфаркта примерно у каждого пятого пациента. Тромб может быть большим и приводить к эмболии. Пациенты часто получают лечение варфарином.

Перикардит
Осложнение инфаркта, поражающее каждого десятого пациента, — воспалительное заболевание сердца перикардит. Он обычно развивается на вторые-четвертые сутки после инфаркта. Проявляется в виде лихорадки с болью в груди. На рентгене грудной клетки иногда можно увидеть шаровидно расширенное сердце. Небольшой перикардит может быть обнаружен с помощью эхокардиографии.
Лечение перикардита проводят с противовоспалительными и обезболивающими препаратами.
Вначале применяют противовоспалительные нестероидные препараты, а стероиды показаны, если признаки серьезны или требуется повторное дренирование.
Депрессия
Изменения психического состояния пациента, как правило, присутствуют в разной степени у пациентов, пострадавших от инфаркта, и отражают плохое состояние головного мозга. Это может быть страх, раздражительность и беспокойство, иногда — гнев, разочарование, печаль и безнадежность, у 65% пациентов присутствуют элементы депрессии, а у 20% пациентов развивается серьезная депрессия.
Инфаркт миокарда увеличивает риск самоубийства. Депрессия после инфаркта миокарда ухудшает общий прогноз выздоровления: у пациентов с депрессией в 3,5 раза выше риск смерти. Этот фактор оказывается часто важнее пола, веса, уровня кровяного давления и холестерина. Однако депрессия диагностируется лишь у четверти пациентов, так как основные ее симптомы похожи на симптомы ишемической болезни сердца, а пациенты в больничной обстановке неохотно жалуются на свое психическое состояние.
Частота осложнений острого инфаркта миокарда постоянно снижается, но смертность от недуга остается на высоком уровне. Детальное знание об осложнениях и их рисках может помочь провести раннюю диагностику, своевременно начать терапию или прибегнуть в случае необходимости к хирургическому вмешательству, чтобы добиться благоприятного исхода.
Нарушения в работе сердца, провоцирующие инфаркт, практически невозможно полностью вылечить. Даже при проведении хирургической операции могут возникнуть ранние и поздние осложнения . Чтобы снизить вероятность развития серьезных патологий, необходимо скорректировать образ жизни, постоянно следить за своим здоровьем.
Осложнения после перенесенного инфаркта возникают на почве нарушения работы сердца, сбоя в процессе перекачивания крови, а также при повышении активности ее свертывания. Многие осложнения являются опасными для жизни. Летальный исход может возникнуть не только в результате инфаркта, но и при несвоевременной диагностике и лечении его последствий.
Осложнения после инфаркта миокарда:
- Образование тромбов.
- Синдром Дресслера.
- Деструкция тканей сердечной мышцы.
- Острая и хроническая сердечная недостаточность.
- Аневризма.
- Кардиогенный шок.
- Нестабильный ритм сердечных сокращений.
К ранним осложнениям инфаркта миокарда относятся левожелудочковая сердечная недостаточность, кардиогенный шок, перикардит, аритмия, а также иные патологии, возникающие в первые часы и дни после инфаркта миокарда.
Тромбоэмболия проявляется при формировании одного или нескольких тромбов. Постепенно сгустки крови передвигаются по сосудам, вызывая закупоривание важных артерий и вен. Впоследствии возникает ишемия определенного органа, также возможно нарушение работы целой системы в организме. После инфаркта в большинстве случаев тромбы образуются в области левого желудочка, аневризменной полости, а также вызывают застой в органах дыхания. Возможно образование атеросклеротических бляшек в ногах, что сопровождается застойными явлениями в нижних конечностях.
Тромболизис необходим для расформирования тромбов. В случае возникновения инфаркта миокарда его проводят в срочном порядке до момента полной нейтрализации некротизированной ткани. Лечение больного может осуществляться в клинике несколько дней, так как в домашних условиях данная процедура не проводится.
Синдром Дресслера
Возникает после инфаркта, характеризуется аутоиммунной природой. Является редким осложнением, однако иногда встречается при прохождении острейшего периода инфаркта. Характерно поражение тканей, которые не имеют прямого отношения к миокарду. Существует несколько вариантов течения синдрома Дресслера.
Перикардит
Патологические процессы в сердечной сумке. Характеризуются следующей симптоматикой:
- Болевой синдром в области грудины.
- Шумы в сердце при проведении соответствующих диагностических мероприятий.
- На ЭКГ диагностируется повышение ST.
Даже при отсутствии лечения проходит в течение 7-14 суток, однако в некоторых случаях осложняется, из-за чего без медикаментозной помощи решить проблему невозможно.
Плеврит
Воспалительный процесс в легочной плевре. Характеризуется следующими признаками:
- Невозможность вдохнуть без боли. Неприятные ощущения усиливаются, если больной сделает глубокий вдох.
- Кашель, осложненный болевым синдромом.
Заболевание можно вылечить в стационарных условиях без возникновения трудностей, однако самостоятельно оно не проходит.
Пневмонит
Воспаление альвеол легких. Одна из наиболее редких патологий, возникающих после инфаркта миокарда. Проявляется такими нарушениями:
- Кашель с отхождением слизи.
- Отсутствие вязкой мокроты, которая указывает на инфекционный процесс.
Необходимо предпринять ряд лечебных мер, так как в противном случае могут возникнуть серьезные осложнения, угроза для жизни.
Синовит
Воспалительный процесс в синовиальных оболочках суставов. В результате патологического процесса образуется излишнее количество жидкости в суставной полости. Заболевание может протекать как самостоятельно, так и проявиться на фоне перечисленных выше патологий. Основные симптомы:
- Болевой синдром без резких спазмов.
- Снижение подвижности суставов при отказе от лечения.
Возможно образование патологий в суставах, расположенных в области плечей, локтей, запястий. Есть вероятность более крупных повреждений. Может пострадать костная ткань в грудине.

Атипичные нарушения
Распространенные патологии:
- Заболевания кожных покровов.
- Патологии сосудистых стенок.
- Нарушения в структуре почек, в том числе развитие недостаточности функций данных органов.
- Одышка, проявляющаяся в первое время после прохождения острой стадии инфаркта миокарда.
Синдром Дресслера проходит без примешивания инфекции, является аутоиммунным заболеванием. Проявляется по причине ошибочного иммунного ответа организма. Возможны патологии как в одном органе, так и в их группе.
При некротизации тканей в крови оказываются вещества, которые должны находиться только в кардиомиоцитах. Некоторые из них являются безопасными для здоровья, однако в некоторых случаях иммунная система воспринимает данные клетки потенциально опасными, из-за чего начинают вырабатываться антитела для их подавления. В результате происходит воспалительный процесс в тканях организма.
Аневризма сердца
Данное заболевание характеризуется острым течением, проявляется при прохождении 14 дней после инфаркта миокарда. Происходит поражение левожелудочковой стенки, из-за чего возникает частичное выпячивание мышечной ткани. Данное нарушение проявляется по причине снижения упругости миокарда. При постоянном оказании давления данный участок растягивается, из-за чего появляется патологический сегмент. Возникает застой крови, так как пораженный участок не сокращается.
Патологии, возникающие по причине аневризмы сердца:
- Разрыв мышечной ткани, провоцирующий сильное кровотечение.
- Нестабильные сокращения сердца, из-за чего возможно возникновение длительных осложнений.
- Развитие сердечной недостаточности.
- Появление тромбов.
Аневризма сердца не всегда проявляется выраженной симптоматикой. В большинстве случаев больные не замечают данного нарушения. Обнаружить аневризму можно только при проведении диагностических исследований. Чтобы вылечить заболевание, необходима медицинская помощь.
Разрыв сердца
Данное нарушение относятся как к ранним, так и к поздним осложнениям инфаркта миокарда. Может осложниться летальным исходом. Нередко разрыв сердца возникает в первую неделю после инфаркта миокарда, однако иногда происходит намного позже. Происходит при деструкции соединительной ткани, из-за чего сердечная мышца не может противостоять внутреннему давлению.
Факторы, способные спровоцировать разрыв сердца:
- Первый инфаркт. Если нарушение происходит во второй или последующие разы, риск разрыва сердца значительно снижается.
- Несоблюдение режима реабилитации, скорректированной лечащим врачом. Особенно опасно сильное физическое перенапряжение.
- Оказание медицинской помощи через сутки или более после возникновения приступа.
- Применение лекарственных препаратов, содержащих глюкокортикоиды, а также нестероидные лекарственные средства, подавляющие процесс рубцевания в области сердца.
Специфического лечения разрыва сердца не существует. Используют лечебные мероприятия, направленные на профилактику разрыва. Их необходимо провести своевременно, соблюдая режим дня.
Сердечная недостаточность
Сердечная недостаточность является опасным последствием инфаркта, может возникнуть через несколько недель после выписки пациента из больницы. Проявляется как в острой, так и в хронической форме. Наиболее опасной считается левожелудочковая недостаточность. Данная патология проявляется при прохождении острого и острейшего периода инфаркта. Наблюдаются острые нарушения в структурах сердца, несущих ответственность за перекачивание крови.
В некоторых случаях люди полагают, что пережили неосложненный инфаркт миокарда, однако постепенно начинают проявляться симптомы сердечной недостаточности, возникшие при таких обстоятельствах:
- Некротизировалась область левого желудочка, занимающая более 15% его площади.
- Произошел некроз сосочковых мышц, необходимых для нормального функционирования митрального клапана.
- Регулярные нарушения ритма сердца.
- Деструкция межжелудочковой перепонки.
При сердечной недостаточности левый желудочек сокращается неправильно, в результате появляются застойные процессы. Стенки растягиваются недостаточно, из-за чего кровь не в полном объеме поступает в диастолу. Происходит клеточное голодание.

При застаивании жидкости в легких возникает отек, интенсивность которого постепенно нарастает. Изначально жидкость находится в капиллярах, затем попадает в альвеолы, что влияет на появление сложностей при дыхании. Если надлежащая помощь будет вовремя отказана, возможна остановка дыхания.
Если сердечная недостаточность протекает в хронической форме, негативные проявления наступают через месяцы, годы после инфаркта. Данная патология возникает при нарушениях функций левого желудочка. Если обнаруживается хроническая форма сердечной недостаточности, данное заболевание не представляет угрозы для жизни.
При сердечной недостаточности нередко появляются приступы кашля, периодически возникает одышка, отеки, человек чувствует слабость, ведет малоподвижный образ жизни. Также возможно головокружение. Потребуется медикаментозная терапия, целью которой является предотвращение более опасных осложнений.
Патологии, при которых больному требуется экстренная помощь, возникают при острой и острейшей стадиях инфаркта миокарда. Чем больше распространяется некроз тканей, тем сильнее болевой синдром. Когда ткань рубцуется, работа сердца восстанавливается, в большинстве случаев наступает улучшение состояния пациента.
Осложнения инфаркта миокарда способны привести к летальному исходу на протяжении первого года жизни после возникновения сердечного приступа. Достаточно часто осложнение при инфаркте миокарда способно унести жизнь человека уже в первые часы после его возникновения. Однако если квалифицированная помощь оказана своевременно, то пациент имеет хорошие шансы на выживаемость.
Классификация осложнений инфаркта
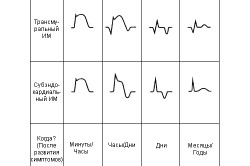
Пациентам, перенесшим приступ, нужно быть готовыми в любое время к появлению осложнений после инфаркта миокарда. Осложнения после инфаркта специалисты классифицируют в зависимости от времени их возникновения на несколько периодов:
- острый;
- подострый;
- постинфарктный.
В отношении первого периода стоит отметить, что он длится на протяжении 10 дней и начинается с первой минуты после приступа. Второй период развития продолжается на протяжении месяца, третий период (постинфарктный) длится в течение полугода. Весь комплекс возникающих при развитии инфаркта осложнений специалисты делят на несколько различных категорий. Этими категориями являются:
- механические;
- электрические;
- эмболические;
- ишемические;
- воспалительные.
 При сердечном приступе развивающиеся патнарушения могут быть двух разновидностей: ранние и поздние.
При сердечном приступе развивающиеся патнарушения могут быть двух разновидностей: ранние и поздние.
Ранние – возникают с первых минут, поздние – появляются в подострый и постинфарктный периоды. К раннему типу осложнений относятся нарушения ритма работы сердца и его проводимости, системы иннервации сердца, развитие , сердечной недостаточности, возникновение разрывов фиброзно-мышечного полого органа. К поздним осложнениям, развивающимся спустя 2-3 недели после возникновения сердечного приступа, относят постинфарктный синдром и хроническую недостаточность кровообращения. Помимо этого, такие нарушения, как аневризма и тромбоэмболия, могут наблюдаться как на ранней стадии развития недуга, так и на поздней.
Наиболее частыми осложнениями, развивающимися при возникновении приступа, являются нарушения сердечного ритма и проводимости системы иннервации сердца. Помимо этого, эти нарушения могут быть единственными проявлениями развития недуга, особенно при развитии повторных. В очень редких случаях у больных может развиваться мерцательная аритмия. При возникновении некротических явлений в значительной массе сердца развиваются трепетание и мерцание желудочков.
Развитие острого периода
Разрыв свободной стенки левого желудка – патнарушение, прогрессирующее при трансмуральной разновидности сердечного приступа. Чаще всего это нарушение наблюдается в первые 5 суток, ликвидируется при помощи хирургического вмешательства.
Тромбоэмболия прогрессирует в течение первых 10 дней развития недуга. При лечении используется гепарин при помощи медленного внутривенного вливания. Дальнейшее лечение осуществляется варфарином.
Отек легких является нарушением, которое прогрессирует в первые 10 дней. Нарушение характеризуется появлением такого расстройства, как кашель. Прогрессирование отека требует немедленной медпомощи. Медики используют для снятия отечности внутривенное введение диуретиков и гликозидов.
В результате перенесения сердечного приступа возможно возникновение психических расстройств.
Клиническое течение инфаркта миокарда нередко отягощается различными осложнениями. Их развитие обусловлено не только размерами поражения, но и комбинацией причин (прежде всего, состоянием миокарда на фоне атеросклероза коронарных артерий, перенесенных ранее болезней миокарда, наличием электролитных нарушений).
Осложнения инфаркта миокарда можно разделить на три основные группы:
Электрические - нарушения ритма и проводимости (брадитахиаритмии, экстрасистолии, внутрижелудочковые и АВ-блокады) - практически постоянные осложнения крупноочагового ИМ. Часто аритмии не являются угрожающими для жизни, но свидетельствуют о серьезных нарушениях (электролитных, продолжающейся ишемии, вагальной гиперактивности и др.), требующих коррекции;
Гемодинамические вследствие нарушений насосной функции сердца (ОЛЖН, ОПЖН и бивентрикулярная недостаточность, КШ, аневризма желудочка, расширение инфаркта); дисфункции сосочковых мышц; механических нарушений (острая митральная регургитация вследствие разрыва сосочковых мышц, разрывы сердца, свободной стенки или межжелудочковой перегородки, аневризмы ЛЖ, отрывы сосочковых мышц); электромеханической диссоциации;
Реактивные и прочие осложнения - эпистенокардический перикардит, тромбоэмболии сосудов малого и большого круга кровообращения, ранняя постинфарктная стенокардия, синдром Дресслера.
По времени появления осложнения инфаркта миокарда классифицируют на:
на ранние осложнения - возникают в первые часы (нередко на этапе транспортировки больного в стационар) или в острейший период (3-4 дня):
1) нарушения ритма и проводимости (90%), вплоть до ФЖ и полной АВ-блокады (самые частые осложнения и причина летальности на догоспитальном этапе). У большей части больных аритмии возникают во время пребывания в отделении интенсивной терапии и реанимации (ОИТР);
2) внезапная остановка сердца;
3) острая недостаточность насосной функции сердца - ОЛЖН и КШ (до 25%);
4) разрывы сердца - наружные, внутренние; медленнотекущие, одномоментные (1-3%);
5) острая дисфункция сосочковых мышц (митральная регургитация);
6) ранний эпистенокардический перикардит;
на поздние осложнения (возникают на 2-3-й неделе, в период активного расширения режима):
1) постинфарктный синдром Дресслера (3%);
2) пристеночный тромбоэндокардит (до 20%);
4) нейротрофические расстройства (плечевой синдром, синдром передней грудной стенки).
Как на ранних, так и на поздних стадиях течения инфаркта миокарда могут возникать острая патология ЖКТ (острые язвы, желудочно-кишечный синдром, кровотечения и др.), психические изменения (депрессия, истерические реакции, психоз), аневризмы сердца (у 3-20% больных), тромбоэмболические осложнения - системные (вследствие пристеночного тромбоза) и ТЭЛА (из-за тромбоза глубоких вен голеней). Так, тромбоэмболии клинически выявляются у 5-10% больных (на аутопсии - у 45%), часто протекают бессимптомно и являются причиной смерти у ряда госпитализированных больных ИМ (до 20%).
У некоторых пожилых мужчин с доброкачественной гипертрофией предстательной железы развивается острая атония мочевого пузыря (снижается его тонус, нет позывов к мочеиспусканию) с увеличением объема пузыря до 2 л, задержкой мочеиспускания на фоне постельного режима и лечения наркотическими ЛС, атропином.
Осложнения инфаркта миокарда, последствия
 Часто инфаркт миокарда протекает с различными осложнениями.
Часто инфаркт миокарда протекает с различными осложнениями.
Развитие этих осложнений продиктовано не только размером площади поражения, но и различными комбинациями причин.
К этим причинам могут относится:
- наличие электролитных нарушений;
- перенесенные ранее болезни миокарда;
- атеросклероз коронарных артерий.
Осложнения инфаркта миокарда
Осложнения инфаркта миокарда подразделяются на три большие группы:
- электрические (нарушения проводимости и ритма);
- гемодинамические;
- реактивные и некоторые другие осложнения.
Время появления осложнений инфаркта миокарда можно классифицировать на:
- ранние осложнения (появляются в первые дни или даже часы заболевания);
- поздние осложнения (появляются через 15-20 дней).
Осложнения острого инфаркта миокарда
Осложнения острого периода инфаркта миокарда включают в себя: острую сердечную недостаточность; нарушения проводимости и сердечного ритма; кардиогенный шок; разрывы сердца (внутренние и наружные); постинфарктный синдром Дресслера; аневризма сердца; эпистенокардитический перикардит; ранняя послеинфарктная стенокардия; тромбэндокардит; тромбэмболические осложнения; нарушения мочеиспускания; осложнения ЖКТ (язвы, эрозии, парез); психические нарушения.
Осложнения после инфаркта миокарда могут быть сформированы очаговым постинфарктным кардиослерозом.
Чаще всего поражению поддается левый желудочек.
Ранние и поздние осложнения инфаркта миокарда.
1. Осложнения острейшего периода ИМ:
а) нарушения ритма сердца — особенно опасны все желудочковые аритмии (желудочковая пароксизмальная тахикардия, политопные желудочковые экстрасистолии и др.), которые могут привести к фибрилляции желудочков и к остановке сердца.
б) нарушения АВ проводимости – чаще возникает при пердне- и заднеперегородочных формах ИМ
в) острая левожелудочковая недостаточность . сердечная астма, отек легких
г) кардиогенный шок — клинический синдром, обусловленный резким падением насосной функции сердца, сосудистой недостаточностью и выраженной дезорганизацией системы микроциркуляции.
Диагностические критерии кардиогенного шока :
1) симптомы недостаточности периферического кровообращения: бледно-цианотичная, «мраморная», влажная кожа; акроцианоз; спавшиеся вены; холодные кисти и стопы; снижение температуры тела; удлинение времени исчезновения белого пятна после надавливания на ноготь > 2 сек
2) нарушение сознания (заторможенность, спутанность сознания, реже – возбуждение)
3) олигурия < 20 мл/ч или анурия
4) САД при двух измерениях < 90 мм.рт. ст. (при предшествовавшей АГ < 100 мм рт.ст.)
5) снижение пульсового АД до 20 мм рт.ст. и ниже
6) снижение среднего АД < 60 мм рт.ст.
7) гемодинамические критерии: сердечный индекс < 2,5 л/мин/м 2 ; давление «заклинивания» в легочной артерии > 15 мм.рт.ст.; повышение ОПСС; снижение ударного и минутного объемов
Купирование кардиогенного шока проводится поэтапно, но в зависимости от формы КШ те или иные мероприятия выполняются в первую очередь:
1. При отсутствии выраженного застоя в легких уложить с приподнятыми под углом 20° нижними конечностями, при застое в легких – положение с приподнятым изголовьем
2. Оксигенотерапия 100% кислородом
3. При выраженном ангинозном приступе (рефлекторная форма КШ ): 1-2 мл 0,005% р-ра фентанила ИЛИ 1 мл 1% р-ра морфина ИЛИ 1 мл 2% р-ра промедола в/в струйно медленно для устранения болевой импульсации + 90-150 мг преднизолона или 150-300 мг гидрокортизона в/в струйно медленно для стабилизации АД
4. В случае аритмической формы КШ при наджелудочковых и желудочковых тахиаритмиях – 5-10 мл 10% р-ра новокаинамида в сочетании с 0,2-0,3 мл 1% р-ра мезатона в/в в течение 5 минут —> нет эффекта 6-10 мл 2% р-ра лидокаина (тримекаина) в/в в течение 5 минут —> нет эффекта —> наркоз тиопенталом натрия, оксибутиратом натрия + ЭИТ, при острой брадиаритмии — 1-2 мл 0,1% р-ра атропина в/в медленно И/ИЛИ 1 мл 0,05% р-ра изадрина или алупента в 200 мл 5% р-ра глюкозы (или физраствора) в/в капельно под контролем АД и ЧСС.
5. При гиповолемии (ЦВД < 80-90 мм водн. ст. – гиповолемическая форма КШ ): 400 мл декстрана/натрия хлорида/ 5% р-ра глюкозы в/в капельно с постепенным увеличением скорости инфузии до исчезновения признаков шока или ЦВД до 120-140 мм вод.ст.
6. При резком снижении насосной функции левого желудочка (истинная форма КШ ):
— допамин 200 мг в 400 мл 5% р-ра глюкозы (физраствора) в/в капельно, начальная скорость введения – 15-20 кап/мин +
— 1-2 мл 0,2% р-ра норадреналина в 200-400 мл 5% р-ра глюкозы (физраствора) в/в капельно под контролем АД, начальная скорость введения – 15-20 кап/мин ИЛИ
— добутамин / добутрекс 250 мг на 250 мл физраствора в/в капельно, начальная скорость введения – 15-20 кап/мин
д) поражения ЖКТ: парез желудка и кишечника (чаще при кардиогенном шоке), стресс-индуцированное желудочное кровотечение
2. Осложнения острого периода – возможны все предыдущие осложнения +:
а) перикардит — возникает при развитии некроза на перикарде обычно на 2-3 день от начала заболевания, при этом усиливаются или вновь появляются боли за грудиной, носящие постоянный пульсирующий характер, усиливающиеся на вдохе, меняющиеся при изменении положения тела и при движениях, аускультативно – шум трения перикарда
б) пристеночный тромбоэндокардит — возникает при трансмуральном ИМ с вовлечением в некротический процесс эндокарда; длительно сохраняются признаки воспаления или они появляются вновь после некоторого спокойного периода; исход процесса — тромбоэмболия в сосуды головного мозга, конечности и в другие сосуды большого круга кровообращения; диагностика: вентрикулография, сцинциграфия миокарда
в) разрывы миокарда:
1) наружный с тампонадой сердца – перед разрывом обычно есть период предвестников в виде рецидивирующих болей, не поддающихся наркотическим анальгетикам; момент разрыва сопровождается сильнейшей болью с потерей сознания, резчайшим цианозом, развитием кардиогенного шока, связанного с тампонадой сердца
2) внутренний разрыв – в виде отрыва папиллярной мышцы (при ИМ задней стенки) с последующим развитием острой клапанной недостаточности (чаще митральной); характерна резчайшая боль, признаки кардиогенного шока, отека легких, пальпаторно систолическое дрожание на верхушке, перкуторно резкое увеличение границ сердца влево, аускультативно грубый систолический шум с эпицентром на верхушке сердца, проводящийся в подмышечную область; в виде разрыва межпредсердной и межжелудочковой перегородок
г) острая аневризма сердца – возникает в период миомаляции при трансмуральном ИМ, наиболее часто расположена в области передней стенки и верхушки левого желудочка; клинически — нарастающая левожелудочковая недостаточность, увеличение границ сердца и его объема, надверхушечная пульсация или симптом коромысла (надверхушечная пульсация + верхушечный толчок), если аневризма формируется на передней стенке сердца; протодиастолический ритм галопа, добавочный III тон, систолический шум; несоответствие между сильной пульсацией сердца и слабым наполнением пульса; «застывшая» ЭКГ с признаками ИМ без характерной динамики; для верификации диагноза показана вентрикулография; лечение оперативное
3. Осложнения подострого периода:
а) хроническая аневризма сердца — возникает в результате растяжения постинфарктного рубца; появляются или долго сохраняются признаки воспаления, характерны увеличение размеров сердца, надверхушечная пульсация, двойной систолический или диастолический шум; на ЭКГ — застывшая форма кривой острой фазы
б) синдром Дресслера (постинфарктный синдром) — связан с сенсибилизацией организма продуктами аутолиза некротизированных масс, появляется не раньше 2-6 нед. от начала заболевания; возникают генерализованные поражения серозных оболочек (полисерозиты), иногда с вовлечением синовиальных оболочек, клинически проявляется перикардитом, плевритом, поражением суставов (чаще всего левого плечевого); перикардит вначале сухой, затем экссудативный, характерны боли за грудиной и в боку (связаны с поражением перикарда и плевры), волнообразная лихорадка, болезненность и припухлость в грудинно-реберных и грудинно-ключичных сочленениях, в ОАК – ускоренное СОЭ, лейкоцитоз, эозинофилия; при назначении ГКС все симптомы быстро исчезают
в) тромбоэмболические осложнения — чаще в малом кругу кровообращения, куда попадают эмболы из вен при тромбофлебите нижних конечностей, вен таза (см. ТЭЛА – вопрос 151).
г) постинфарктная стенокардия
4. Осложнения хронического периода: постинфарктный кардиосклероз – исход ИМ, связанный с формированием рубца; проявляется нарушениями ритма, проводимости, сократимости миокарда
24. Артериальная гипертензия: этиология, патогенез, клинические проявления, диагностика, классификация, принципы лечения. План обследования на амбулаторном этапе.
Артериальная гипертензия – стабильное повышение АД – систолического до величины ³ 140 мм рт.ст. и/или диастолического до величины ³ 90 мм рт.ст. по данным не менее чем двукратных измерений по методу Короткова при двух или более последовательных визитах пациента с интервалом не менее 1 недели.
Среди артериальных гипертензий выделяют:
а) первичная АГ (эссенциальная, гипертоническая болезнь, 80% всех АГ) — повышение АД – основной, иногда единственный, симптом заболевания, не связанный с органическим поражением органов и систем, регулирующих АД.
б) вторичная АГ (симптоматическая, 20% всех АГ) – повышение АД обусловлено почечными, эндокринными, гемодинамическими, нейрогенными и другими причинами.
Эпидемиология: АГ регистрируется у 15-20% взрослых; с возрастом частота повышается (в 50-55 лет – у 50-60%);
Основные этиологические факторы эссенциальной АГ.
а) наследственная предрасположенность (мутации генов ангиотензиногена, альдостеронсинтетазы, натриевых каналов почечного эпителия, эндотелина и др.)
б) острое и хроническое психоэмоциональное перенапряжение
в) избыточного потребление поваренной соли
г) недостаточное поступление с пищей кальция и магния
д) вредные привычки (курение, злоупотребление алкоголем)
е) ожирение
ж) низкая физическая активность, гиподинамия
Основные факторы и механизмы патогенез эссенциальной АГ .
1. Полигенная наследственная предрасположенность ® дефект плазматической мембраны ряда клеток с нарушением ее структуры и ионотранспортной функции —> нарушение функции Na + /K + -АТФ-азы, кальциевых насосов ® задержка Na + и жидкости в сосудистой стенке, увеличение внутриклеточного содержания Ca 2+ ® гипертонус и гиперреактивность ГМК сосудов.
2. Нарушение равновесия между прессорными (катехоламины, факторы РААС, АДГ) и депрессорными (предсердный натрийуретический гормон, эндотелиальный релаксирующий фактор — оксид азота, простациклины) факторами.
3. Психоэмоциональное перенапряжение —> формирование в коре головного мозга очага застойного возбуждения ® нарушение деятельности центров сосудистого тонуса в гипоталамусе и продолговатом мозге ® выделение катехоламинов ®
а) чрезмерное усиление симпатических вазоконстрикторных влияний на α 1 -адренорецепторы резистивных сосудов —> повышение ОПСС (пусковой механизм).
б) усиление синтеза белка, роста кардиомиоцитов и ГМК и их гипертрофия
в) сужение почечных артерий ® ишемия почечной ткани —> гиперпродукция ренина клетками юкстагломерулярного аппарата —> активация ренин-ангиотензиновой системы ® выработка ангиотензина II ® вазоконстрикция, гипертрофия миокарда, стимуляция выработки альдостерона (в свою очередь альдостерон способствует задержке натрия и воды в организме и секреции АДГ с дальнейшим накоплением жидкости в сосудистом русле)
Вышеперечисленные механизмы вызывают повышение АД . которое приводит к:
1. гипертрофии стенок артерий и миокарда ® развитие относительной коронарной недостаточности (т.к. рост капилляров миокарда не успевает за ростом кардиомиоцитов) ® хроническая ишемия —> рост соединительной ткани —> диффузный кардиосклероз.
2. длительному спазму почечных сосудов ® гиалиноз, артериолосклероз —> первично-сморщенная почка ® ХПН
3. хронической цереброваскулярной недостаточности —> энцефалопатия и т.д.
В случае поражения артерии, кровоснабжающей синусовый узел, возможно развитие дисфункции синусового узла. Это осложнение более вероятно в том случае, если существовало предшествовавшее поражение синусового узла (часто встречающееся среди пожилых). Синусовая брадикардия, наиболее частая дисфункция синусового узла, обычно не требует лечения, за исключением случаев артериальной гипотензии или ЧСС
Постоянная синусовая тахикардия обычно является угрожающим симптомом, часто свидетельствует о недостаточности левого желудочка низком сердечном выбросе. При отсутствии левожелудочковой недостаточности или другой очевидной причины этот вариант аритмии может ответить на введение b-адреноблокаторов внутривенно или внутрь в зависимости от степени экстренности.
Предсердные аритмии
Предсердные нарушения ритма (предсердная экстрасистолия, мерцательная аритмия и реже трепетание предсердий) развиваются приблизительно у 10 % больных инфарктом миокарда и могут отражать наличие левожелудочковой недостаточности или инфарктом миокарда правого предсердия. Пароксизмальная предсердная тахикардия встречается редко и обычно у больных, имевших подобные эпизоды ранее. Предсердная экстрасистолия обычно протекает доброкачественно, однако считают, что увеличение частоты может приводить к развитию сердечной недостаточности. Частая предсердная экстрасистолия может быть чувствительна к назначению b-адреноблокаторов.
Мерцательная аритмия обычно бывает преходящей, если возникает в первые 24 ч. Факторы риска включают возраст более 70 лет, сердечную недостаточность, перенесенные ранее инфаркты миокарда, обширный предшествующий инфаркт миокарда, инфаркт предсердий, перикардит, гипокалиемию, гипомагниемию, хронические заболевания легких и гипоксию. Применение фибринолитических средств снижает вероятность развития данного осложнения. Повторяющиеся пароксизмы мерцательной аритмии - плохой прогностический фактор, увеличивающий риск системных эмболии.
При мерцательной аритмии обычно назначают гепарин натрия, поскольку существует риск системных эмболии. Внутривенное введение b-адреноблокаторов (например, атенолол от 2,5 до 5,0 мг в течение 2 мин до достижения к полной дозы 10 мг за 10-15 мин, метопролол от 2 до 5 мг каждые 2-5 мин до полной дозы 15 мг за 10-15 мин) замедляет частоту желудочковых сокращений. Необходим тщательный контроль ЧСС и АД. Лечение прекращают при выраженном снижении ЧСС или систолическом АД QRS, можно рассматривать внутривенное введение верапамила или дилтиазема. Последний препарат можно назначать в виде внутривенных введений для поддержания нормальной ЧСС длительное время.
Если мерцательная аритмия нарушает системную циркуляцию (например, приводя к развитию левожелудочковой недостаточности, артериальной гипотензии или боли в груди), показана экстренная кардиоверсия. В случае повторения мерцательной аритмии после кардиоверсии следует рассмотреть возможность внутривенного введения амиодарона.
При трепетании предсердий ЧСС контролируют так же, как и при мерцательной аритмии, однако не вводят гепарин натрия.
Из наджелудочковых тахиаритмии (если не учитывать синусовую тахикардию) в остром периоде инфаркта миокарда чаще всего наблюдается мерцание предсердий - у 10-20% больных. Все остальные варианты наджелудочковых тахикардии при инфаркте миокарда встречаются очень редко. При необходимости проводятся стандартные лечебные мероприятия.
Ранняя мерцательная аритмия (в первые сутки инфаркта миокарда), как правило, носит преходящий характер, ее возникновение связывают с ишемией предсердий и эпистенокардическим перикардитом. Возникновение мерцательной аритмии в более поздние сроки в большинстве случаев является следствием растяжения левого предсердия у больных с дисфункцией левого желудочка (аритмия сердечной недостаточности). При отсутствии заметных нарушений гемодинамики мерцание предсердий не требует проведения лечебных мероприятий. При наличии выраженных нарушений гемодинамики методом выбора является проведение неотложной электрической кардиоверсии. При более стабильном состоянии возможны 2 варианта ведения больных: (1) урежение ЧСС при тахисистолической форме в среднем до 70 в мин с помощью в/в введения бета-блокаторов, дигоксина, верапамила или дилтиазема; (2) попытка восстановления синусового ритма с помощью в/в введения амиодарона или соталола. Преимуществом второго варианта является возможность достижения восстановления синусового ритма и одновременно быстрое урежение ЧСС в случае сохранения мерцания предсердий. У больных с явной сердечной недостаточностью выбор проводится между двумя препаратами: дигоксин (в/в введение около 1 мг дробными дозами) илиамиодарон (в/в 150-450 мг). Всем больным с мерцанием предсердий показано в/в введение гепарина.
Брадиаритмии
Нарушение функции синусового узла и атриовентрикулярные блокады чаще наблюдаются при инфаркте миокарда нижней локализации, особенно в первые часы. Синусовая брадикардия редко представляет какие-либо проблемы. При сочетании синусовой брадикардии с выраженной гипотонией («синдром брадикардии-гипотонии») используют внутривенное введение атропина.
Атриовентрикулярные (АВ) блокады также чаще регистрируются у больных с нижним инфарктом миокарда.
На ЭКГ отмечаются признаки острого коронарного синдрома с подъемом сегмента STII, III, aVF (в отведенииях I, aVL, V1-V5 отмечается реципрокная депрессия сегмента ST). У больного полная АВ-блокада, ритм АВ-соединения с частотой 40 в мин.
Частота возникновения АВ-блокады П-Ш степени при нижнем инфаркте миокарда достигает 20%, а если имеется сопутствующий инфаркт миокарда правого желудочка - АВ-блокада отмечается у 45-75% больных. АВ-блокада при инфаркте миокарда нижней локализации, как правило, развивается постепенно: сначала удлинение интервала PR, затем АВ-блокада II степени типа I (Мобитц-1, периодика Самойлова-Венкебаха) и только после этого - полная АВ-блокада. Даже полная АВ-блокада при нижнем инфаркте миокарда почти всегда носит преходящий характер и продолжается от нескольких часов до 3-7 сут (у 60% больных - менее 1 сут). Однако возникновение АВ-блокады является признаком более выраженного поражения: госпитальная летальность при неосложненном нижнем инфаркте миокарда составляет 2-10%, а при возникновении АВ-блокады достигает 20% и более. Причиной смерти при этом является не сама АВ-блокада, а сердечная недостаточность, вследствие более обширного поражения миокарда.
На ЭКГ регистрируется подъем сегмента ST в отведениях II, III, aVF и в V1-V3. Подъем сегмента ST в отведениях V1-V3 является признаком вовлечения правого желудочка. В отведениях I, aVL, V4-V6 отмечается реципрокная депрессия сегмента ST. У больного полная АВ-блокада, ритм АВ-соединения с частотой 30 в мин (в предсердиях синусовая тахикардия с частотой 100/мин).
У больных с нижним инфарктом миокарда при возникновении полной АВ-блокады выскальзывающий ритм из АВ-соединения, как правило, обеспечивает полную компенсацию, существенных нарушений гемодинамики обычно не отмечается. Поэтому лечения в большинстве случаев не требуется. При резком снижении ЧСС - менее 40 в мин и возникновении признаков недостаточности кровообращения используют в/в введение атропина (по 0,75-1,0 мг, при необходимости повторно, максимальная доза составляет 2-3 мг). Представляют интерес сообщения об эффективности в/в введения аминофиллина (эуфиллина) при АВ-блокадах, резистентных к атропину («атропин-резистентные» АВ-блокады). В редких случаях может потребоваться инфузия бета-2-стимуляторов: адреналина, изопротеренола, алупента, астмопента или ингаляция бета-2-стимуляторов. Необходимость в проведении электрокардиостимуляции возникает крайне редко. Исключение представляют случаи нижнего инфаркта миокарда с вовлечением правого желудочка, когда при правожелудочковой недостаточности в сочетании с выраженной гипотонией для стабилизации гемодинамики может потребоваться проведение двухкамерной электростимуляции, т.к. при инфаркте миокарда правого желудочка очень важно сохранение систолы правого предсердия.
При инфаркте миокарда передней локализации АВ-блокада II-III степени развивается только у больных с очень массивным поражением миокарда. При этом АВ-блокада происходит на уровне системы Гиса-Пуркинье. Прогноз у таких больных очень плохой - смертность достигает 80-90% (как при кардиогенном шоке). Причиной смерти является сердечная недостаточность, вплоть до развития кардиогенного шока или вторичная фибрилляция желудочков.
Предвестниками возникновения АВ-блокады при переднем инфаркте миокарда являются: внезапное появление блокады правой ножки пучка Гиса, отклонение электрической оси и удлинение интервала PR. При наличии всех трех признаков вероятность возникновения полной АВ-блокады составляет около 40%. В случаях возникновения этих признаков или регистрации АВ-блокады II степени типа II (Мобитц-II) показано профилактическое введение стимуляционного зонда-электрода в правый желудочек. Средством выбора для лечения полной АВ-блокады на уровне ветвей пучка Гиса с медленным идиовентрикулярным ритмом и гипотонией является временная электрокардиостимуляция. При отсутствии кардиостимулятора используют инфузию адреналина (2-10 мкг/мин), возможно применение инфузии изадрина, астмопента или сальбутамола со скоростью, обеспечивающей достаточное увеличение ЧСС. К сожалению, даже в случаях восстановления АВ-проводимости прогноз у таких больных остается неблагоприятным, летальность значительно повышена как во время пребывания в стационаре, так и после выписки (по некоторым данным, летальность в течение первого года достигает 65%). Правда, в последние годы появились сообщения, что после выписки из стационара факт преходящей полной АВ-блокады уже не влияет на отдаленный прогноз больных с передним инфарктом миокарда.
Нарушения проводимости
Блокада типа Мобитц I (блокада Венкебаха, прогрессирующее удлинение интервала PR) часто развивается при нижнедиафрагмальном инфаркте миокарда; она редко прогрессирует. Блокада типа Мобитц II (редкие сокращения) обычно указывает на наличие массивного переднего инфаркта миокарда, так же как и полная атриовентрикулярная блокада с широкими комплексами QRS (предсердные импульсы не достигают желудочков), но оба типа блокад встречаются нечасто. Частота полных (III степени) АВ-блокад зависит от локализации инфаркта. Полная АВ-блокада встречается у 5-10 % больных с нижним инфарктом миокарда и обычно бывает преходящей. Она возникает менее чем у 5 % пациентов с неосложненным передним инфарктом миокарда, но до 26 % при таком же виде инфаркта миокарда, сопровождающегося блокадой правой или задней ветви левой ножек пучка Гиса.
Блокада типа Мобитц I обычно не требует лечения. В случае развития истинной блокады типа Мобитц II низкой ЧСС или при АВ-блокаде с редкими широкими комплексами QRS применяют временный кардиостимулятор. Можно использовать внешний кардиостимулятор до имплантации временного кардиостимулятора. Несмотря на то что введение изопротеренола может временно восстановить ритм и ЧСС, этот подход не используют, поскольку происходит увеличение потребности миокарда в кислороде и риска развития аритмий. Атропин в дозе 0,5 мг каждые 3-5 мин до достижения полной дозы 2,5 мг можно назначить при наличии АВ-блокады с узким желудочковым комплексом и небольшой ЧСС, но он не рекомендован при АВ-блокаде с впервые возникшим широким желудочковым комплексом.
Желудочковые аритмии
Чаще всего при инфаркте миокарда отмечается желудочковая экстрасистолия.
До недавнего времени желудочковой экстрасистолии при инфаркте миокарда придавали очень большое значение. Популярной была концепция так называемых «предупреждающих аритмий», согласно которой желудочковые экстрасистолы высоких градаций (частые, полиморфные, групповые и ранние - типа «R на Т») являются предвестниками фибрилляции желудочков, а лечение желудочковых экстрасистол должно способствовать снижению частоты возникновения фибрилляции. Концепция «предупреждающих аритмий» не подтвердилась. В настоящее время установлено, что экстрасистолы, возникающие при инфаркте миокарда, сами по себе безопасны (их даже называют «косметической аритмией») и не являются предвестниками фибрилляции желудочков. А самое главное - лечение экстрасистолии не влияет на частоту возникновения фибрилляции желудочков.
В рекомендациях Американской кардиологической ассоциации по лечению острого инфаркта миокарда (1996 г.) было специально подчеркнуто, что регистрация желудочковых экстрасистол и даже неустойчивой желудочковой тахикардии (включая полиморфную желудочковую тахикардию, продолжительностью до 5 комплексов) не является показанием для назначения антиаритмических препаратов(!). Отрицательное прогностическое значение имеет выявление частых желудочковых экстрасистол через 1-1,5 сут от начала инфаркта миокарда, т.к. в этих случаях желудочковые экстрасистолы являются «вторичными» и, как правило, возникают вследствие обширного поражения и выраженной дисфункции левого желудочка («маркеры дисфункции левого желудочка»).
Неустойчивая желудочковая тахикардия
Неустойчивой желудочковой тахикардией называют эпизоды желудочковой тахикардии, продолжительностью менее 30 с («пробежки» тахикардии), не сопровождающиеся нарушениями гемодинамики. Многие авторы неустойчивую желудочковую тахикардию так же, как и желудочковую экстрасистолию, относят к «косметическим аритмиям» (их называют «энтузиастическими» выскальзывающими ритмами»).
Антиаритмические препараты назначают только при очень частых, обычно групповых экстрасистолах и неустойчивой желудочковой тахикардии, если они вызывают нарушения гемодинамики с возникновением клинических симптомов или субъективно очень плохо переносится больными. Клиническая ситуация при инфаркте миокарда очень динамична, аритмии часто носят преходящий характер, и очень трудно провести оценку эффективности лечебных мероприятий. Тем не менее в настоящее время рекомендуется избегать применения антиаритмических препаратов класса I (за исключением лидокаина), а при наличии показаний для антиаритмической терапии предпочтение отдается бета-блокаторам, амиодарону и, возможно, соталолу.
Лидокаин вводят внутривенно - 200 мг в течение 20 мин (обычно повторными болюсами по 50 мг). При необходимости проводят инфузию со скоростью 1-4 мг/мин. При отсутствии эффекта от лидокаина, чаще применяют бета-блокаторы или амиодарон. В России в настоящее время наиболее доступным бета-блокатором для внутривенного введения является пропранолол (обзидан). Обзидан при инфаркте миокарда вводят со скоростью 1 мг в течение 5 мин. Доза обзидана при в/в введении составляет от 1 до 5 мг. При наличии эффекта переходят на прием бета-блокаторов внутрь. Амиодарон (кордарон) вводят внутривенно медленно в дозе 150-450 мг. Скорость введения амиодарона при длительной инфузии составляет 0,5-1,0 мг/мин.
Устойчивая желудочковая тахикардия
Частота возникновения устойчивой желудочковой тахикардии (тахикардия, которая не проходит спонтанно) в остром периоде инфаркта миокарда достигает 15%. В случае возникновения выраженных нарушений гемодинамики (сердечная астма, гипотония, потеря сознания) методом выбора является проведение электрической кардиоверсии разрядом 75-100 Дж. При более стабильном состоянии гемодинамики прежде всего применяют лидокаин или амиодарон. В нескольких исследованиях показано преимущество амиодарона перед лидокаином в купировании желудочковых тахиаритмий. Если желудочковая тахикардия продолжается, то при сохранении стабильной гемодинамики можно продолжить эмпирический подбор терапии, например, оценить эффект в/в введения обзидана, соталола, магния сульфата или провести плановую электрическую кардиоверсию.
Интервал между введением различных препаратов зависит от состояния больного и при хорошей переносимости тахикардии, отсутствии признаков ишемии и относительно стабильной гемодинамике составляет от 20-30 мин до нескольких часов.
Для лечения полиморфной желудочковой тахикардии типа «пируэт» препаратом выбора является сульфат магния - в/в введение 1-2 г в течение 2 мин (при необходимости повторно) и последующая инфузия со скоростью 10-50 мг/мин. При отсутствии эффекта от сульфата магния у больных без удлинения интервала QT (в синусовых комплексах) оценивают действие бета-блокаторов и амиодарона. При наличии удлинения интервала QT используют электрокардиостимуляцию с частотой около 100/мин. Следует отметить, что у больных с острым инфарктом миокарда даже при удлинении интервала QT в лечение тахикардии типа «пируэт» может быть эффективно применение бета-блокаторов и амиодарона.
Фибрилляция желудочков
Известно, что приблизительно 50% всех случаев фибрилляции желудочков происходят в первый час инфаркта миокарда, 60% - в первые 4 часа, 80% - в первые 12 часов инфаркта миокарда.
Если ускорить вызов врача скорой помощи на 30 мин, можно предотвратить примерно 9% случаев смерти от фибрилляции желудочков за счет своевременной дефибрилляции. Это намного превышает эффект от тромболитической терапии.
Частота возникновения фибрилляции желудочков после поступления больного в блок интенсивной терапии составляет 4,5-7%. К сожалению, в 1-й час поступают менее 20% больных, в течение 2-х часов - около 40%. Расчеты показывают, что если ускорить поступление больных на 30 мин, можно будет спасти от фибрилляции примерно 9 больных из 100. В основном это так называемая первичная фибрилляция желудочков (не связанная с рецидивированием инфаркта миокарда, ишемией и недостаточностью кровообращения).
Единственным эффективным методом лечения фибрилляции желудочков является немедленное проведение электрической дефибрилляции. При отсутствии дефибриллятора реанимационные мероприятия при фибрилляции желудочков практически всегда безуспешны, более того, с каждой минутой снижается вероятность успешной электрической дефибрилляции. Эффективность немедленной электрической дефибрилляции при инфаркте миокарда составляет около 90%.
Прогноз у больных, перенесших первичную фибрилляцию желудочков, как правило, вполне благоприятный и, по некоторым данным, практически не отличается от прогноза у больных с неосложненным инфарктом миокарда. Фибрилляция желудочков, возникающая в более поздние сроки (после первых суток), в большинстве случаев является вторичной и обычно возникает у больных с выраженным поражением миокарда, рецидивирующими инфарктами миокарда, ишемией миокарда или признаками сердечной недостаточности. Следует отметить, что вторичная фибрилляция желудочков может наблюдаться и в течение первых суток инфаркта миокарда. Неблагоприятный прогноз при этом определяется тяжестью поражения миокарда. Частота возникновения вторичной фибрилляции желудочков составляет 2,2-7%, в т. ч. у 60% в первые 12 ч. У 25% больных вторичная фибрилляция желудочков отмечается на фоне мерцания предсердий. Эффективность дефибрилляции при вторичной фибрилляции составляет от 20 до 50%, повторные эпизоды возникают у 50% больных, летальность больных в стационаре составляет 40-50%. Имеются сообщения, что после выписки из стационара наличие в анамнезе даже вторичной фибрилляции желудочков уже не оказывает дополнительного влияния на прогноз.
Проведение тромболической терапии позволяет резко (в десятки раз) снизить частоту возникновения устойчивой желудочковой тахикардии и вторичной фибрилляции желудочков. Реперфузионные аритмии не представляют проблемы, в основном это частые желудочковые экстрасистолы и ускоренный идиовентрикулярный ритм («косметические аритмии») - показатель успешного тромболизиса. Редко возникающие более серьезные аритмии, как правило, хорошо поддаются стандартной терапии.
Сердечная недостаточность
Больные с обширным инфарктом миокарда (по данным ЭКГ или сывороточным маркерам) и нарушением сократительной способности миокарда, АГ или диастолической дисфункцией более склонны к развитию сердечной недостаточности. Клинические проявления зависят от размера инфаркта, увеличения давления наполнения левого желудочкаи степени снижения сердечного выброса. Часто возникают одышка, инспираторные хрипы в нижних отделах легких и гипоксемия.
Сердечная недостаточность при инфаркте миокарда
Основной причиной смерти больных инфарктом миокарда в стационаре является острая сердечная недостаточность: отек легких и кардиогенный шок.
Клиническими проявлениями острой левожелудочковой недостаточности являются одышка, ортопноэ, ощущение нехватки воздуха, вплоть до удушья, повышенная потливость. При объективном обследовании отмечаются бледность, цианоз, увеличение частоты дыхания, нередко набухание шейных вен. При аускультации - разнообразные хрипы в легких (от крепитирующих до влажных крупнопузырчатых), III тон (протодиастолический ритм галопа), систолический шум. В большинстве случаев отмечаются синусовая тахикардия и снижение АД, пульс слабого наполнения или нитевидный.
При инфаркте миокарда используют классификацию острой сердечной недостаточности по Киллипу: I класс - нет застойных явлений, II класс-признаки умеренных застойных явлений: хрипы в нижних отделах легких, выслушивание III тона или умеренная правожелудочковая недостаточность (набухание вен шеи и увеличение печени), III класс - отек легких, IV класс - кардиогенный шок.
Характерные клинические проявления сердечной недостаточности наблюдаются при достаточно выраженной степени недостаточности кровообращения, когда ее «легче диагностировать, чем лечить». Раннее выявление сердечной недостаточности по клиническим признакам представляет очень трудную задачу (клинические проявления на ранних стадиях неспецифичны и не очень точно отражают состояние гемодинамики). Синусовая тахикардия может быть единственным признаком компенсированной недостаточности кровообращения (компенсация за счет синусовой тахикардии). К группе больных с повышенным риском возникновения недостаточности кровообращения относятся больные с распространенным инфарктом миокарда передней локализации, с повторным инфарктом миокарда, с АВ-блокадами II-III степени при наличии нижнего инфаркта миокарда (или с признаками вовлечения правого желудочка, с выраженной депрессией сегмента ST в передних отведениях), больные с мерцательной аритмией или выраженными желудочковыми аритмиями, нарушениями внутрижелудочковой проводимости.
Идеальным считается всем больным с повышенным риском или начальными признаками сердечной недостаточности проводить инвазивное мони-торирование гемодинамики. Для этой цели удобнее всего использовать «плавающие» катетеры Сван-Ганца. После введения катетера в легочную артерию измеряют так называемое «заклинивающее» давление в ветвях легочной артерии или диастолическое давление в легочной артерии. Используя метод термодилюции, можно вычислить сердечный выброс. Применение инвазивного контроля гемодинамики значительно облегчает выбор и проведение лечебных мероприятий при острой сердечной недостаточности. Для обеспечения адекватной гемодинамики у больных с острым инфарктом миокарда диастолическое давление в легочной артерии (отражает давление заполнения левого желудочка) должно быть в пределах от 15 до 22 мм рт. ст. (в среднем около 20 мм). Если диастолическое давление в легочной артерии (ДДЛА) менее 15 мм рт. ст. (или даже в пределах от 15 до 18 мм) - причиной недостаточности кровообращения или фактором, способствующим ее появлению, может быть гиповолемия. В этих случаях на фоне введения жидкости (плазмозамещающих растворов) отмечается улучшение гемодинамики и состояния больных. При кардиогенном шоке отмечается снижение сердечного выброса (сердечный индекс меньше 1,8-2,0 л/мин/м 2) и повышение давления заполнения левого желудочка (ДДЛА больше 15-18 мм рт. ст., если нет сопутствующей гиповолемии). Однако ситуация, при которой имеется возможность инвазивного контроля гемодинамики для большинства учреждений практического здравоохранения (тем более в условиях скорой помощи), действительно является идеальной, т.е. такой, которой не существует в действительности.
При умеренно выраженной сердечной недостаточности, клинически проявляющейся небольшой одышкой, крепитирующими хрипами в нижних отделах легких, при нормальном или слегка повышенном АД используют нитраты (нитроглицерин под язык, нитраты внутрь). На этом этапе очень важно не «перелечить», т.е. не вызвать чрезмерного снижения давления заполнения левого желудочка. Используют назначение малых доз ингибиторов АПФ, реже применяют фуросемид (лазикс). У нитратов и ингибиторов АПФ есть преимущество перед диуретиками - они снижают преднагрузку без уменьшения ОЦК.
Последовательность лечебных мероприятий при появлении клинических признаков сердечной астмы или отека легких:
- ингаляция кислорода,
- нитроглицерин (под язык повторно или в/в),
- морфин (в/в по 2-5 мг),
- лазикс (в/в по 20-40 мг и более),
- дыхание с положительным давлением на выдохе,
- искусственная вентиляция легких.
Даже при развернутой клинической картине отека легких после сублингвального приема 2-3 таблеток нитроглицерина может быть заметный положительный эффект уже через 10 мин. Вместо морфина можно использовать другие наркотические анальгетики и/или реланиум. Лазикс (фуросемид) при отеке легких у больных с инфарктом миокарда используют в последнюю очередь, осторожно, начиная с 20 мг, если сохраняется выраженная одышка, при необходимости увеличивая дозу в 2 раза при каждом повторном введении. При отеке легких у больных с инфарктом миокарда, как правило, нет задержки жидкости, поэтому при передозировке лазикса может развиться выраженная гиповолемия и гипотония.
В некоторых случаях достаточно применения только одного из препаратов (чаще всего нитроглицерина), иногда приходится вводить все 3 препарата почти одновременно, не дожидаясь появления эффекта от каждого средства в отдельности. Ингаляцию кислорода проводят с увлажнением, пропуская через стерильную воду или спирт. При выраженном пенообразовании можно проколоть трахею тонкой иглой и ввести 2-3 мл 96° спирта.
При возникновении отека легких на фоне повышенного АД лечебные мероприятия почти такие же, как и при нормальном АД. Однако при резком повышении АД или сохранении высокого АД, несмотря на введение нитроглицерина, морфина и лазикса, дополнительно используют дроперидол, пентамин, инфузию нитропруссида натрия.
Отек легких на фоне снижения АД - особенно тяжелое состояние. Это кардиогенный шок с преобладанием симптомов застоя в легких. В этих случаях нитроглицерин, морфин и лазикс применяют в уменьшенных дозах на фоне инфузии инотропных и вазопрессорных препаратов: добутамин, допамин или норадреналин. При незначительном снижении АД (около 100 мм рт. ст.) можно начать с инфузии добутамина (с 200 мкг/мин, при необходимости повышая скорость введения до 700-1000 мкг/мин). При более резком снижении АД используют допамин (150-300 мкг/мин). При еще более выраженном снижении АД (менее 70 мм рт. ст.) показано введение норадреналина (с 2-4 мкг/мин до 15 мкг/мин) или проведение внутриаортальной баллонной контрпульсации. Глюкокортикоидные гормоны при кардиогенном отеке легких не показаны.
Лечение зависит от степени тяжести. При умеренно выраженной сердечной недостаточности назначают петлевые диуретики (например, фуросемид от 20 до 40 мг внутривенно 1 раз в день) для уменьшения давления заполнения желудочков, и этого часто бывает достаточно. В тяжелых случаях используют вазодилататоры (например, внутривенное введение нитроглицерина) для уменьшения пред- и постнагрузки; во время лечения часто измеряют давление заклинивания легочной артерии путем катетеризации правых камер сердца (с использованием катетера Суона-Ганца). Ингибиторы АПФ используют до тех пор, пока систолическое АД остается выше 100 мм рт. ст. Для начала терапии предпочтительнее назначение ингибиторов АПФ короткого действия в малых дозах (например, каптоприл по 3,125-6,25 мг каждые 4-6 ч, увеличивая дозу по переносимости). Как только максимальная доза достигнута (максимум для каптоприла составляет 50 мг 2 раза в день), назначают ингибитор АПФ более длительного действия (например, фозиноприл, лизиноприл, рамиприл) на продолжительное время. Если сердечная недостаточность сохраняется на уровне II функционального класса по NYHA либо более высокого класса, необходимо добавить антагонисты альдостерона (например, эплеренон или спиронолактон). При тяжелой сердечной недостаточности применяют внутриартериальную баллонную контр-пульсацию для обеспечения временной гемодинамической поддержки. В тех случаях, когда невозможно выполнить реваскуляризацию или хирургическую коррекцию, рассматривают вопрос о пересадке сердца. Долговременные левожелудочковые или бивентрикулярные имплантируемые устройства можно использовать до трансплантации; если пересадка сердца невозможна, эти вспомогательные устройства иногда применяет в качестве постоянного метода лечения. Иногда использование таких устройств приводит к восстановлению функций желудочков, и устройство может быть удалено через 3-6 мес.
Если сердечная недостаточность приводит к развитию гипоксемии, назначают ингаляции кислорода через носовые катетеры (для поддержания раО на уровне приблизительно 100 мм рт. ст.). Это может способствовать оксигенации миокарда и ограничению зоны ишемии.
Поражения папиллярных мышц
Функциональная недостаточность папиллярных мышц возникает приблизительно у 35 % больных в течение первых нескольких часов инфаркта. Ишемия папиллярных мышц приводит к неполному смыканию створок митрального клапана, что затем проходит у большинства больных. Однако у некоторых пациентов появление рубцов в папиллярных мышцах или свободной стенке сердца приводит к постоянной митральной регургитации. Функциональная недостаточность папиллярных мышц проявляется поздним систолическим шумом и обычно исчезает без лечения.
Разрыв папиллярной мышцы наиболее часто возникает при нижнезаднем инфаркте миокарда, связанном с окклюзией правой венечной артерии. Это приводит к появлению острой выраженной митральной регургитации. Разрыв папиллярной мышцы характеризуется внезапным появлением громкого голосистолического шума и дрожания на верхушке, обычно с отеком легкого. В некоторых случаях, когда регургитация не вызывает интенсивной аускультативной симптоматики, но клинически возникает подозрение на это осложнение, выполняют эхокардиографию. Эффективный метод лечения - пластика или замена митрального клапана.
Разрыв миокарда
Разрыв межжелудочковой перегородки или свободной стенки желудочка происходит у 1 % больных с острым инфарктом миокарда и становится причиной 15 % госпитальной летальности.
Разрыв межжелудочковой перегородки, тоже будучи редким осложнением, встречается в 8-10 раз чаще, чем разрыв папиллярной мышцы. Разрыв межжелудочковой перегородки характеризуется внезапным появлением громкого систолического шума и дрожания, определяемых на уровне от середины до верхушки сердца, вдоль левого края грудины на уровне третьего и четвертого межреберных промежугков, сопровождается артериальной гипотензией с признаками недостаточности левого желудочкаили без них. Диагноз может быть подтвержден при использовании катетеризации баллонным катетером и сравнении сатурации О2 или рО2 в правом предсердии, правом желудочкеи отделах легочной артерии. Существенное увеличение рО2 в правом желудочке диагностически значимо, как и данные допплеровской эхокардиографии. Лечение хирургическое, оно должно быть отсрочено на 6 нед после инфаркта миокарда, поскольку необходимо максимальное заживление поврежденного миокарда. Если сохраняется выраженная гемодинамическая нестабильность, проводят более раннее хирургическое вмешательство, несмотря на высокий риск смертности.
Частота разрывов свободной стенки желудочка увеличивается с возрастом, чаще такой разрыв происходит у женщин. Это осложнение характеризуется внезапным падением артериального давления с сохранением синусового ритма и (часто) признаками тампонады сердца. Хирургическое лечение редко бывает успешным. Разрыв свободной стенки почти всегда бывает фатальным.
Аневризма желудочка
Ограниченное выбухание стенки желудочка, чаще левого, может происходить в зоне обширного инфаркта миокарда. Аневризма желудочка часто встречается при больших трансмуральных инфарктов миокарда (обычно передних). Аневризма может развиваться через несколько дней, недель или месяцев после инфаркта миокарда. Разрыв аневризм происходит редко, однако они могут приводить к рецидивирующим желудочковым аритмиям, низкому сердечному выбросу и пристеночному тромбозу с системной эмболией. Аневризму желудочков подозревают, когда выявляются парадоксальные движения в прекардиальной области. ЭКГ демонстрирует постоянный подъем сегмента ST, а рентгенологическое исследование грудной клетки выявляет характерную выпуклость сердечной тени. Для подтверждения диагноза и выявления тромбов выполняют эхокардиографию. При наличии левожелудочковой недостаточности или аритмии можно назначить хирургическое иссечение. Применение ингибиторов АПФ во время острого инфаркта миокарда уменьшает ремоделирование миокарда и может снижать частоту развития аневризм.
Псевдоаневризма представляет собой неполный разрыв свободной стенки левого желудочка, ограничивающийся перикардом. Псевдоаневризмы почти всегда содержат тромбы и часто разрываются полностью. Лечение проводят хирургическим путем.
Артериальная гипотензия и кардиогенный шок
Артериальная гипотензия может быть обусловлена уменьшенным наполнением желудочков или снижением силы сокращения вследствие обширного инфаркта миокарда. Значимую артериальную гипотензию (систолическое АД
Уменьшение наполнения левого желудочканаиболее часто вызвано уменьшенным венозным возвратом, обусловленным гиповолемией, особенно у больных, получающих интенсивную терапию петлевыми диуретиками, однако оно может быть признаком инфаркта миокарда правого желудочка. Выраженный отек легких свидетельствует о потере силы сокращений левого желудочка (левожелудочковая недостаточность), ставшей причиной шока. Лечение зависит от причины этого состояния. У некоторых больных для выяснения причины необходима катетеризация легочной артерии для измерения внутрисердечного давления. Если давление заклинивания легочной артерии ниже 18 мм рт. ст., более вероятно уменьшение наполнения, связанное с гиповолемией; если давление выше 18 мм рт. ст., вероятна левожелудочковая недостаточность. При артериальной гипотензии, связанной с гиповолемией, возможна осторожная заместительная терапия 0,9 % раствором натрия хлорида без развития перегрузки левых камер сердца (чрезмерного повышения давления в левом предсердии). Однако иногда функционирование левого желудочка настолько изменено, что возмещение жидкости резко увеличивает давление заклинивания легочной артерии до уровня, характерного для отека легких (> 25 мм рт. ст.). Если давление в левом предсердии высокое, артериальная гипотензия, вероятно, связана с недостаточностью левого желудочка, и при неэффекгивности диуретиков может требоваться инотропная терапия или поддержка адекватного кровообращения.
При кардиогенном шоке временно эффективными могут быть а- или b-агонисты. Допамин, катехоламин, воздействующий на рецепторы и назначают в дозе 0,5-1 мкг/кг в минуту с ее увеличением до достижения удовлетворительного ответа либо до достижения дозы приблизительно 10 мкг/кг в минуту. Более высокие дозы стимулируют вазоконстрикцию и вызывают предсердные и желудочковые аритмии. Добутамин, а-агонист, можно назначать внутривенно в дозе 2,5-10 мкг/кг в минуту или больше. Это часто приводит к развитию артериальной гипотензии или усиливает ее. Назначение наиболее эффективно в том случае, когда гипотензия обусловлена низким сердечным выбросом с высоким периферическим сопротивлением сосудов. Допамин может быть более эффективен, чем добутамин, когда необходим вазопрессорный эффект. В рефрактерных случаях возможно использование комбинации допамина и добутамина. Как временную меру можно использовать внутриаортальную баллонную контрпульсацию. Направленный лизис тромба, ангиопластика или экстренное АКШ могут существенно улучшать функции желудочка. НОВА или АКШ рассматривают при сохраняющейся ишемии, рефрактерной желудочковой аритмии, гемодинамической нестабильности или шоке, если анатомические особенности артерий это позволяют.
Ишемия или инфаркт миокарда правого желудочка
Примерно у половины больных с нижним инфарктом миокарда имеется вовлечение правого желудочка, в т. ч. у 15-20% гемодинамически значимое. Клинически у таких больных наблюдается гипотония или шок в сочетании с признаками венозного застоя в большом круге: набухание вен шеи, увеличение печени, периферические отеки (признаки венозного застоя могут отсутствовать при сопутствующей гиповолемии и появиться после инфузии жидкости). «Классическая триада инфаркта миокарда правого желудочка»: набухание шейных вен, отсутствие застоя в легких и гипотония. Кроме этого, отмечается выраженная одышка без ортопноэ. Клиническая картина напоминает тампонаду сердца, констриктивный перикардит, тромбоэмболию легочной артерии. При инфаркте миокарда правого желудочка более часто возникает АВ-блокада II-III степени и мерцание предсердий. Одним из признаков вовлечения правого желудочка является резкое снижение АД, вплоть до обморока, при приеме нитроглицерина.
На ЭКГ-признаки инфаркта миокарда, обычно нижней локализации, а в отведении V1 и в правых грудных отведениях (VR4-R6) регистрируется подъем сегмента ST. В случае вовлечения задне-базальных отделов левого желудочка в отведениях V1-V2 наблюдается депрессия сегмента ST и увеличение высоты зубца R. При зондировании правых отделов сердца отмечается повышение давления в правом предсердии и желудочке (диастолическое более 10 мм рт. ст.). При эхокардиографии наблюдается нарушение сократимости и увеличение размеров правого желудочка, отсутствие значительного выпота в полости перикарда и тампонады.
Основным способом лечения гипотонии при инфаркте миокарда правого желудочка является в/в введение жидкости («объем-зависимый инфаркт миокарда»). Инфузию плазмозамещающих растворов (физраствор, реополиглюкин) проводят со скоростью, обеспечивающей повышение диастолического давления в легочной артерии до 20 мм рт. ст. или АД до 90-100 мм рт. ст. (при этом признаки венозного застоя в большом круге и ЦВД нарастают) - единственная «движущая сила» при инфаркте миокарда правого желудочка - повышенное давление в правом предсердии. Первые 500 мл вводят струйно (болюсом). В некоторых случаях приходится вводить несколько литров плазмозамещающих растворов - до 1-2 литров за 1-2 часа (по словам одного из кардиологов: «необходимо лить жидкость, вплоть до анасарки»).
При появлении признаков застоя в легких скорость инфузии уменьшают или введение плазмозамещающих растворов прекращают. При недостаточном эффекте от инфузии жидкости к лечению добавляют добутамин (допамин или норадреналин). В самых тяжелых случаях применяют внутриаортальную контрпульсацию.
Противопоказано назначение вазодилататоров (включая нитроглицерин и наркотические анальгетики) и диуретиков. Под влияние этих препаратов наблюдается резкое снижение АД. Повышенная чувствительность к действию нитратов, морфина и диуретиков является диагностическим признаком инфаркта миокарда правого желудочка. Самым эффективным способом лечения инфаркта миокарда с вовлечением правого желудочка является восстановление коронарного кровотока (тромболитическая терапия или хирургическая реваскуляризация). Прогноз при правильном лечении больных с инфарктом миокарда правого желудочка в большинстве случаев вполне благоприятный, улучшение функции правого желудочка отмечается в первые 2-3 сут, а признаки застоя в большом круге обычно исчезают в течение 2-3 нед. При правильном лечении прогноз зависит от состояния левого желудочка.
Тяжелым и, к сожалению, нередко наблюдающимся осложнением при инфаркте миокарда правого желудочка является полная АВ-блокада. В этих случаях может потребоваться проведение двухкамерной электрокардиостимуляции, т. к. при инфаркте миокарда правого желудочка очень важное значение имеет сохранение эффективной систолы правого предсердия. При отсутствии возможности двухкамерной электрокардиостимуляции применяют внутривенное введение эуфиллина и электростимуляцию желудочков.
Таким образом, выявление и своевременная коррекция трех курабельных состояний: рефлекторной гипотонии, гиповолемии и инфаркта миокарда правого желудочка позволяет добиться существенного улучшения в этой группе больных даже при клинической картине шока. Не менее важно и то, что неправильное лечение, например применение вазопрессоров при гиповолемии, вазодилататоров или диуретиков при инфаркте миокарда правого желудочка, нередко является причиной ускорения летального исхода.
Продолжающаяся ишемия
Любая боль в груди, которая сохраняется или повторяется в течение 12-24 ч после инфаркта миокарда, может быть проявлением продолжающейся ишемии. Постинфарктная ишемическая боль указывает, что сохраняется риск развития инфаркта больших участков миокарда. Обычно продолжающуюся ишемию можно идентифицировать по обратимым изменения интервала ST-T на электрокардиограмме; возможно повышение АД. Однако, поскольку продолжающаяся ишемия может быть безболевой (изменения данных ЭКГ при отсутствии болевого синдрома) приблизительно у трети больных обычно назначают серию ЭКГ через каждые 8 ч в первый день и далее ежедневно. При продолжающейся ишемии лечение аналогично нестабильной стенокардии. Прием нитроглицерина под язык или внутривенно обычно эффективен. Для сохранения ишемизированного миокарда целесообразно рассмотреть вопрос о коронарной ангиопластике и НОВА или АКШ.
Пристеночный тромбоз
Пристеночный тромбоз развивается приблизительно у 20 % больных с острым инфарктом миокарда. Системную эмболию выявляют приблизительно у 10 % больных с тромбами в левом желудочке. Риск наиболее высок в первые 10 дней, но сохраняется по крайней мере в течение 3 мес. Наиболее высокий риск (более 60 %) у больных с обширным передним инфарктом миокарда (особенно с вовлечением дистальных отделов межжелудочковой перегородки и верхушки), расширенным левым желудочкоми распространенными зонами гипокинеза либо постоянной мерцательной аритмией. Для уменьшения риска эмболии назначают антикоагулянты. При отсутствии противопоказаний внутривенно вводят гепарин натрия, назначают внутрь варфарин на 3-6 мес с поддержанием MHO между 2 и 3. Антикоагулянтную терапию проводят длительно, если у больного расширенный с распространенными зонами гипокинеза левого желудочка, аневризма левого желудочкаили постоянная мерцательная аритмия. Также возможет длительный прием ацетилсалициловой кислоты.
Перикардит
Перикардит развивается вследствие распространения некроза миокарда через стенку желудочка на эпикард. Это осложнение развивается приблизительно у трети больных с острым трансмуральным инфарктом миокарда. Шум трения перикарда обычно появляется начиная с 24 до 96 ч после дебюта инфаркта миокарда. Более раннее появление шума трения необычно, хотя геморрагический перикардит иногда осложняет раннюю стадию инфаркта миокарда. Острая тампонада развивается редко. Перикардит диагностируют с помощью ЭКГ, которая демонстрирует диффузный подъем сегмента STn (иногда) депрессию интервала PR. Эхокардиографию выполняют часто, но обычно данные бывают нормальными. Иногда выявляют небольшое количество жидкости в перикарде или даже бессимптомную тампонаду. Прием ацетилсалициловой кислоты или других НПВС обычно уменьшает проявления. Высокие дозы или дпительное использование НПВС либо глюкокортикоидов могут тормозить заживление инфаркта, что необходимо учитывать.
Постинфарктный синдром (синдром Дресслера)
Постинфарктный синдром развивается у некоторых пациентов через несколько дней, недель или даже месяцев после острого инфаркта миокарда. В последние годы отмечают уменьшение частоты его развития. Синдром характеризуется лихорадкой, перикардитом с шумом трения перикарда, появлением жидкости в перикарде, плевритом, жидкостью в плевральной полости, легочными инфильтратами и распространенной болью. Этот синдром вызван аутоиммунной реакцией на некротическую ткань миоцитов. Он может повторяться. Дифференциальная диагностика постинфарктного синдрома с прогрессированием или повторением инфаркта миокарда может быть затруднительной. Однако при постинфарктном синдроме не происходит заметного увеличения количества кардиоспецифических маркеров, и изменения данных ЭКГ неопределенные. НПВС обычно эффективны, но синдром может повторяться несколько раз. В тяжелых случаях может потребоваться короткий интенсивный курс другого НПВС или глюкокортикоида. Высокие дозы НПВС или глюкокортикоида не используют дольше нескольких дней, поскольку они могут препятствовать раннему заживлению желудочка после острого инфаркта миокарда.






